Vorbemerkung
Der vorliegende Artikel war ursprünglich als Nachtrag zu bereits veröffentlichten mineralogischen Untersuchungen (SCHUSTER 1992) in der Todsburger Höhle geplant. Er basiert auf Geländearbeiten, die schon im Sommer 1992 durchgeführt und zur Veröffentlichung in einer süddeutschen karstkundlichen Schriftenreihe eingereicht worden waren. Diese Zeitschrift ist jedoch nie erschienen und um zu verhindern, dass die gewonnenen Erkenntnisse verloren gehen, legt der Verfasser den Bericht nun hier der Öffentlichkeit vor. Leider fielen die Originale der beiden Infrarot-Spektren, auf die im Text bezug genommen wird, der Redaktion jener ursprünglichen Zeitschrift zum Opfer und können nicht mehr ohne weiteres rekonstruiert werden. Der Text enthält jedoch glücklicherweise eine schriftliche Auswertung, so dass der Verlust verschmerzbar ist.
Zum besseren Verständnis werden außerdem einige Hinweise aus dem bereits publizierten ersten Teil (SCHUSTER 1992) kurz wiederholt.
1. Einleitung
1990 und 1991 waren aus der Todsburger Höhle Mineralproben entnommen und analysiert worden. Besonders musste ein Mineralgemenge hervorgehoben werden, das in Form eines schwarzen, pastösen Überzuges an einer Stelle der Höhle auf der Bodensinterschicht aufsitzt. Naßchemische Untersuchungen wiesen in diesem Gemenge Calcit und Eisenoxidhydrate nach. Dazu kommen unlösliche Bestandteile, die zunächst als Quarz und Korund angesprochen wurden, mengenmäßig jedoch nicht mehr quantifiziert werden konnten.
Mit rund 37 % stellen organische Stoffe unbekannter Zusammensetzung einen weiteren erheblichen Massenanteil dar. In der Anhand der Analyse hergeleiteten Theorie zur Entstehung dieses Mineralgemischs, spielt die organische Komponente eine zentrale Rolle, nach der dreiwertiges Eisen durch diese Substanzen zu einer zweiwertigen, wasserlöslichen Form reduziert wurde (SCHUSTER 1992).
Am 18.07.1992 zogen M. Feth und der Verfasser in der Todsburger Höhle letztmalig eine kleine Probe der mineralischen Substanz. Die Ergebnisse der Auswertung vermögen einige der Lücken zu schließen und auch die Entstehungstheorie kann an einigen Punkten verfeinert werden.
2. Entnahmepunkt
Die Fundstelle des Mineralgemenges liegt in einem der niedrigen Seitenteile, die den Hauptgang der Todsburger Höhle über weite Strecken begleiten. Etwa auf der Höhe der ersten Wasserpfütze nach der Eingangshalle, kann man rechts (S) in eine solche nischenartige Seitenpassage hineinschlufen, die sich auf einer Querkluft entwickelt hat. Hier überzieht der schwarze Belag mehrere Quadratmeter Bodenfläche.
Im ersten Augenblick wurde dieser Überzug spontan als Fackelruß interpretiert, jedoch nach der Überlegung, warum das Material nur den Boden bedeckt, die Decke aber sauber ist, wurde die Neugier der Bearbeiter geweckt und Probensubstanz entnommen.
3. Labormethoden
3.1. Frühere Untersuchungen
1991 wurden bereits Tests durchgeführt und deren Ergebnisse als erster Zwischenbericht 1992 von SCHUSTER publiziert. Dabei stellte sich heraus, dass ein großer prozentualer Anteil der Probenmasse in Mineralsäuren löslich ist. In der Lösung wurde Calcium durch komplexometrische Titration bestimmt, dreiwertiges Eisen durch Spektralphotometrie und gleichfalls komplexometrisch der Versuch geführt, Magnesium nachzuweisen. Letzteres verlief negativ. Die Titrationstechniken sind in A.A. (o.J.) detailliert beschrieben.
Die schwarzen, farbgebenden Massen jedoch stellten sich als säureunlöslich heraus und wurden zur Weiterverarbeitung abfiltriert und bei rd. 900°C und Zutritt von Luftsauerstoff geglüht. Die Rückstände verflüchtigten sich dabei fast vollständig und zurück blieben kleine Mengen weißer und hellgrauer Mineralkörnchen mit z.T. großer Härte. Daraus folgt, dass die schwarze Substanz offensichtlich eine Kohlenstoffverbindung organischer Natur ist.
Aufgrund der Tatsache, dass die Probe Eisen enthält, das in seiner vorliegenden, dreiwertigen Form sehr schwer in Wasser löslich ist und also ein spezieller Transportmechanismus vorgelegen haben muss, damit das Eisen dennoch in das Höhlensediment gelangen konnte, wurde darüber nachgedacht, ob ein Zusammenhang mit der organischen Substanz bestehen könnte. Die späteren Untersuchungen, die der eigentliche Bestandteil dieses Aufsatzes sind, scheinen dies zu belegen.
3.2. Aktuelle Untersuchungen
Um detaillierten Aufschluß über den Mineralbestand in der Probe zu erhalten, fiel die Wahl des Analysenverfahrens auf die infrarotspektroskopische Standardmethode für Feststoffe.
Die z.T. chemisch aufbereiteten Proben, bei rd. 100°C getrocknet, wurden jeweils mit einem etwa zehnfachen Massenüberschuß von trockenem Kaliumbromid p.a. in einer hydraulischen Presse unter Vakuum zu klaren Tabletten verdichtet. Diese Preßlinge konnten dann teilweise in herkömmlichen IR-Spektrometern durchgemessen werden, wozu die erhaltenen Spektren manuell auf Übereinstimmung mit Vergleichsspektren von Reinsubstanzen geprüft wurden; teilweise war es auch möglich, die Probanden auf dem Laser-IR aufzuscannen und die Transmissionskurven per Computerdatenbank automatisch mit Vergleichsmaterial zu überlagern.
Zur Feinuntersuchung der organischen Stoffe, wobei besonderes Interesse dem Nachweis funktioneller Gruppen galt, die Eisenverbindungen reduzieren können, kam versuchsweise die Dünnschichtchromatographie zum Einsatz.
Als Elutionsmittel kamen drei verschiedene Gemische mit unterschiedlich ausgeprägter Polarität zur Anwendung:
- Toluol/ Ethanol/ Ammoniak- Gemisch
- Toluol/ Ameisensäure/ Diethylether- Gemisch
- Petrolether/ Diethylether- Gemisch
Nachdem die Proben auf die DC- Platten aufgetragen waren, ließ man im Entwicklungstank, z.T. mehrmals, das Fließmittel bis knapp unter die Oberkante aufsteigen und nach dem Trocknen wurden die Chromatogramme zur Detektion der evtl. vorhandenen Spots mit den Sprühreagenzien Platinat, Ninhydrin, Echtblau B und Diethylaminobenzaldehyd behandelt (TREIBER 1984).
Eine Identifizierung einzelner Verbindungen ist nach dieser Methode unmöglich, jedoch konnte prinzipiell durch die unterschiedlichen Rf– Werte eine Auftrennung in verschiedene Substanzzonen erwartet werden, in denen sich funktionelle Gruppen besser als in der Mischung, mit ihren sich gegenseitig störenden Komponenten, nachweisen lassen.
4. Ergebnisse
4.1. Auswertung der IR-Spektrogramme
Es wurde zunächst von einer unbehandelten Probe ein Spektrogramm aufgezeichnet, das die Werte der IR- Transmission gegenüber der Wellenzahl (cm-1) wiedergibt. Schon die chemische Analyse hatte für Calcit einen Massenanteil von knapp zwei Dritteln in der Mineralmischung ausgewiesen (SCHUSTER 1992: 70); dieser Sachverhalt findet im Spektrum seinen Niederschlag in Form der sehr intensiven Absorptionsbanden des Calciumcarbonats.
Als charakteristisch sind die Peaks bei den Wellenzahlen 3400 cm-1, 2900 cm-1, 2500 cm-1, 1790 cm-1, 870 cm-1, 710 cm-1 und ganz besonders bei 1430 cm-1 hervorzuheben. Damit wird unverkennbar Calcit angezeigt.
Daneben tritt jedoch auch Absorption im Bereich 3500- 3700 cm-1 und vor allem bei 1040 cm-1 auf, die nicht dem Kalkspat zuzuschreiben ist.
Da die CaCO3– Banden die übrigen Peaks zu stark überdecken, wurde in einer weiteren Probe der Calcitanteil durch milde Säurebehandlung entfernt und nur der unlösliche Rückstand spektroskopiert. Das hieraus resultierende Spektrum konnte in der Mehrheit aller Punkte mit einem Vergleichsspektrum des SiO2 (Quarzsand) aus der Datenbank in Einklang gebracht werden. Als Charakteristika gelten die Peaks bei 3500 cm-1, 2950 cm-1, 2880 cm-1(schwach ausgeprägt), 2350 cm-1, 1650 cm-1 1040 cm-1 (hier handelt es sich um den sehr intensiven Peak, der auch im Spektrum der unbehandelten Probe auftritt) und 700 cm-1. Damit ist das bereits vermutete Vorkommen von Quarz gesichert.
Allerdings treten im Verlauf der Spektralkurve der Probe zusätzliche Peaks auf, die sich im Quarz- Vergleichsspektrum nicht wiederfinden lassen. Es handelt sich um die Absorptionslinien bei 3700 cm-1, 3600 cm-1, 900 cm-1 und 800 cm-1. Durch ein entsprechendes Vergleichsspektrum konnte damit darüber hinaus noch Kaolinit identifiziert werden.
4.2. Auswertung der Dünnschichtchromatogramme
Die in die Dünnschichtchromatographie gesetzten Erwartungen haben sich nicht erfüllt. Der Versuch, die organischen Komponenten aus der Probe abzutrennen und über Dünnschichtchromatographie weiter aufzuschließen, scheiterte an deren mangelhaften bzw. fehlenden Löslichkeit in den benutzten Elutionsmitteln. Darum brachte auch die Behandlung der entwickelten Platten mit Sprühreagenzien keine positiven Resultate.
5. Diskussion
Die IR-Spektroskopie konnte die Zusammensetzung der anorganischen, mineralischen Komponenten des Mineralaggregats, wie diese bereits aus den chemischen Analysenergebnissen schlußfolgert worden war, in praktisch allen Punkten bestätigen.
Während das Vorhandensein von Calcit schon nach der naßchemischen Untersuchung feststand, brachte erst die Spektralanalytik den gesicherten Quarz- Nachweis. Dieses Mineral war bislang nur aufgrund von extrem hitze- und säurebeständigen Kristallen, die in der Probe gefunden worden waren, vermutet worden. Dagegen stellte sich der Verdacht, dass auch Al2O3 mit enthalten sein könnte, als Irrtum heraus. Die IR- Spektroskopie lieferte keinerlei Anzeichen für Korund, dafür aber eindeutig für Kaolinit.
Kaolinit ist ein Vertreter der Tonminerale, ein Zweischichtsilikat mit der Zusammensetzung Al2Si2O5(OH)4. Es geht z.B. aus der Verwitterung von Feldspat hervor, wobei dieser Abbauprozeß in zwei Stufen abläuft:
Zunächst erfolgt durch die Einwirkung von Hydroxoniumionen die sogenannte „Entbasung“:
2 KAlSi3O8 + 2 H3O+ —> 2 HAlSi3O8 + 2 H2O + 2 K+
Durch Wasseranlagerung entstehen Kaolinit und Kieselsäure.
2 HAlSi3O8 + 5 H2O —> Al2Si2O5(OH)4 + 4 H2SiO3
Indes gilt es die Abhängigkeit der Löslichkeit von SiO2 und Al3+ vom pH- Wert zu beachten (Abb. 1). Im pH- Bereich 5- 9 liegt unlösliches Al(OH)3 vor, das bei Prozessen innerhalb dieser Grenzen der Mineralneubildung somit nicht zur Verfügung steht. Bei pH < 5 geht Al3+als Hexaquokomplex in Lösung, bei pH > 9 geht es in den löslichen Tetrahydroxoaluminat- Komplex über.

Die Löslichkeit des SiO2 nimmt dagegen mit steigendem pH-Wert annähernd linear zu. Daher entstehen Si-ärmere Zweischichtsilikate wie Kaolinit bevorzugt bei tiefen pH- Werten, wo zwar viel Al3+ in der Lösung zur Verfügung steht, aber im Vergleich dazu ein SiO2– Unterschuß herrscht.
In diesem Zusammenhang ist auf die erste Reaktionsgleichung zu verweisen, aus der ersichtlich ist, dass die Feldspatverwitterung in Gegenwart von H3O+, also im sauren Bereich, abläuft. ZIECHMANN & MÜLLER- WEGENER (1990: 218) benennen einen „Silikat- Pufferbereich“, der zwischen dem Carbonat- Pufferbereich und dem Austauscher- Bereich liegt, also bei einem pH- Wert von ca. 5.
Darüber hinaus ist der Verwitterungsprozeß klimagesteuert; Kaolinit bildet sich bevorzugt unter feuchten und kühlen Bedingungen (siallitische Verwitterung). Leider liegen keine zuverlässigen Angaben vor, so dass es nicht möglich ist, anhand von bekannten Klimadaten eine Altersabschätzung zu treffen. Am ehesten kommt das Ende des Würm- Glazials als Entstehungszeitraum für diese Mineralmixtur in Frage (kühle bis kalte Witterung, jedoch genügend flüssiges Wasser, um die Verwitterung und Umlagerung in die Höhle zu bewerkstelligen). Diese Beobachtung deckt sich gut mit den radiometrisch gewonnenen Altersangaben des Sinters aus der Todsburger Höhle, der sich im Postglazial gebildet hat (FRANKE, MÜNNICH & VOGEL 1959): Das auf dem Bodensinter liegende Material mussjünger sein als der Sinter.
Bereits früher (SCHUSTER 1992) wurden in dem Mineralaggregat basische Eisenoxide durch naßchemisch- photometrische Untersuchungen nachgewiesen. Eine exakte Strukturanalyse war nicht möglich. Definitionsgemäß wurden die Eisenminerale als Limonitangesprochen. „Limonit“ ist ein Sammelbegriff für diverse Eisenoxide und -Hydrate wechselnder Konstitution. Meistens wird er mit der Formel FeOOH bzw. Fe(OH)3zusammengefaßt, was streng genommen nicht ganz richtig ist.
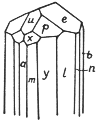
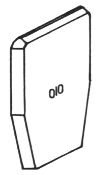
Von FeOOH sind zwei verschiedene Modifikationen bekannt: alpha – FeOOH oder Goethit und gamma – FeOOH oder Lepidokrokit. Ersteres ist auch als „Nadeleisenerz“, letzteres als „Rubinglimmer“ bekannt. Die Kristallformen beider Modifikationen sind aus den Abb. 2 und 3 (nach KLOCKMANN 1980: 553/ 554) ersichtlich. Lepidokrokit ist bei normalen Temperaturen metastabil und wandelt sich langsam in den weitaus häufigeren Goethit um. KLOCKMANN (1980 :553) teilt mit:
"Goethit mit seinen Varietäten ist ein typisches Produkt der Verwitterungszone (...) unter Einfluß von Humussäuren, gelöstes Eisen wird in dieser Form gefällt. (...) Limonit oder 'Brauneisenerz' schlechthin (...) besteht überwiegend aus Goethit."
Zur Erklärung der Entstehung der FeOOH-Ablagerungen wurde die Theorie herangezogen, dass Huminstoffe mit elektrophoben Gruppen (z.B. die Carbonyl- Gruppe) das Eisen des FeOOH zur zweiwertigen Form reduzieren, die durch das größere Löslichkeitsprodukt eine höhere Mobilität in Wasser besitzt und deshalb zur Umlagerung von der Erdoberfläche in die Höhle in Betracht kommt. Aus Abb. 1 geht hervor, dass die Löslichkeit von Eisen bei pH- Werten über 3 rapide abnimmt (Ausfällung von schwerlöslichem Fe(OH)3).
Die Analyse von Tropfwässern aus Höhlen ergab aber einen durchschnittlichen pH 7,4 (SIMMLEIT 1987: 31). Auch Karstgrundwasser aus dem Karbonatkarst hat einen annähernd neutralen pH- Wert; im Frankendolomit z.B. von 7,4 (FREVERT ET AL. 1982: 65). Das Löslichkeitsprodukt von FeOOH liegt bei diesem Wert nur bei 2,5 10-42 mol4 l-4 (nach KÜSTER 1985), so dass praktisch kein Transport von gelöstem Eisen stattfindet.
Die Kohlensäure alleine reicht keinesfalls aus, um pH 3 oder tiefer zu erreichen, auch dann nicht, wenn man den in der Bodenluft erhöhten CO2– Partialdruck berücksichtigt. Der Humusboden in Karbonatkarstgebieten enthält viel Kalk, welcher mit Kohlensäure ein leistungsfähiges Puffersystem bildet. ZIECHMANN & MÜLLER- WEGENER (1990: 216) berechnen den tiefsten möglichen pH- Wert des Bodenwassers mit 6,2. Die hier wiedergegebene Tabelle der beiden Autoren zeigt jedoch, dass durch die Pufferwirkung des CaCO3 die pH- Werte i.d.R. noch deutlich höher liegen.
Tabelle 1: pH- Werte in Abhängigkeit vom CO2– Partialdruck (aus ZIECHMANN & MÜLLER- WEGENER 1990: 216)
| Böden | CO2– Partialdruck [hPa] | |||
| 0,3 | 1 | 10 | 100 | |
| Natriumboden | 9,0 | 8,6 | 7,9 | 7,2 |
| Boden mit 9 % CaCO3 | 8,3 | 8,0 | 7,4 | 6,7 |
| CaCO3– freier Boden | 6,9 | 6,7 | 6,4 | 6,0 |
| dest. Wasser | 5,7 | 5,4 | 4,9 | 4,4 |
Neben der Kohlensäure muss im Erdreich ein weiterer Protonendonator vorhanden sein, um die für die Eisenlösung idealen Säurewerte zu erreichen. Auch die Feldspatverwitterung läuft in saurem Milieu ab. "Durch das Überwiegen von Phenol- und Carbonylgruppen sind Huminsäuren echte Säuren, die einer Salzbildung fähig sind (Humate)"(ZIECHMANN & MÜLLER- WEGENER 1990: 52).
Dies verdeutlicht, dass die organischen Stoffe, deren Reste noch in dem Mineralgemenge mit einem Massenanteil von 37 % vorhanden sind, eine wesentlich bedeutendere Rolle für die Mineralbildung spielen, als ursprünglich angenommen. Sie sind nicht nurReduktionsmittel, sondern auch Puffersubstanz für die Eisenlösung und die Feldspatverwitterung.
Die nachgewiesenen Überreste im Mineralgemenge passen ganz ins Bild, denn derartige Zersetzungsprozesse sind in der Literatur beschrieben: "...doch ist ihre Wirkung begrenzt, da sie allmählich durch Mikroorganismen und Luftsauerstoffeinwirkung in CO2 und H2O umgewandelt werden" (RÖMPP, S. 1521).
Huminstoffe sind ausgeprägte Chelatbildner; d.h. sie bilden besonders mit Nebengruppenmetallen wie z.B. Eisen, lösliche Komplexverbindungen. In dieser Form können die Metalle leicht als Lösung transportiert werden. Die Inkohlungsprozesse nach der Ablagerung in der Höhle setzen das Metalloxid/ -hydroxid durch oxidative Zerstörung des Chelats wieder frei.
Zusammenfassend lässt sich formulieren, dass
- die Existenz der Minerale Calcit, Quarz, Kaolinit und Limonit/ Goethit in einem sedimentären Mineralgemenge in der Todsburger Höhle als gesichert gelten kann.
- Huminsäuren eine entscheidende Rolle bei der Mineralgenese spielten, da sie einerseits die H3O+– Ionen für die Feldspatverwitterung und die Fe- Lösung liefern und andererseits als Komplexbildner und Reduktionsmittel für den Transport in die Höhle sorgen.
- die Entstehung des Materials vermutlich nach dem Ende der letzten Eiszeit erfolgte.
Nachbemerkung
Aufgrund der vorliegenden Befunde werden die Vorgänge, die zur Bildung der Mineralisation in der Todsburger Höhle geführt haben, als rein abiotische Prozesse gewertet. Sowohl die Umsetzung der Minerale an der Erdoberfläche als auch die oxidative Ausfällung im Höhleninnern können durch Redoxreaktionen aus der organischen und anorganischen Chemie erklärt werden. Jedoch, seit einer ganzen Reihe von Jahren, mehren sich die Hinweise darauf, dass erhebliche Teile der Eisen- und Manganerze in sedimentären Lagerstätten als direkte Lebensäußerungen von Mikroorganismen (vor allem Bakterien, aber auch Eukarioten) zu deuten sind. Aktuelle Ergebnisse sind in MENNE (1996) und in SKINNER & FITZPATRICK (1992) dokumentiert.
Inwiefern dies auch auf die hier besprochenen Minerale aus der Todsburger Höhle anzuwenden ist, kann beim gegenwärtigen Untersuchungsstand nicht entschieden werden. Die Oxidation der Fe+II– haltigen Lösung in der Höhle kann durch Beteiligung von Mikroorganismen erfolgen, muss jedoch nicht. Ebenso wahrscheinlich ist die in diesem Aufsatz zur Diskussion gestellte abiotische Fällung der Minerale durch die pH- und eH- Änderung in der Lösung, nachdem diese in den lufterfüllten Hohlraum eingetreten ist. Die in den Augen des Verfassers viel interessantere Frage, welche Vorgänge im einzelnen im Boden über der Höhle die Lösung des dreiwertigen Eisens herbeigeführt haben, bleibt durch die Mikrobiologie vorerst unbeantwortet. Die Reduktion und Mobilisierung des Eisens erfordert Energie- warum sollte ein Mikroorganismus Energie für einen für ihn nutzlosen, ja sogar schädlichen Vorgang aufbringen? Eisen ist in höheren Konzentrationen toxisch, also müsste ein Bakterium „Interesse“ daran haben, dieses Element durch Fällung aus seiner Umwelt zu beseitigen, statt die Konzentration durch Auflösung noch zu erhöhen. Sicherlich richtig ist aber die indirekte Beteiligung von Organismen an der Eisenreduktion durch die Bereitstellung von reduzierenden organischen Stoffwechselprodukten.
Dank
Ein besonderes Wort des Dankes möchte ich MARTIN FETH aussprechen, der die zeitraubenden IR- spektroskopischen Aufnahmen durchführte und somit die Realisierung dieses Berichts überhaupt erst ermöglicht hat.
Literatur
A.A. (o.J.): Komplexometrische Bestimmungsmethoden mit Titriplex.- 111 S.; Darmstadt.-[Analysensammlung, herausgegeben von Fa. E. Merck].
FRANKE, H.W. & MÜNNICH, K.O. & VOGEL, J.C. (1959): Erste Ergebnisse von Kohlenstoff- Isotopenmessungen an Kalksinter.- Die Höhle, 10(2): 17- 22; Wien.
FREVERT, T. & SCHRIMPFF, E. & BAUMGARTNER, I. (1982): Kalk- Kohlensäure- Gleichgewicht in oberflächennahen Grundwässern NO- Bayerns.- Z. Wasser Abwasser Forsch., 15(2): 58- 69, 1 Abb., 3 Tab.; Weinheim.
KLOCKMANN, F. (1980): Klockmanns Lehrbuch der Mineralogie.- 16. Aufl., 876 + 55 S., 631 Abb.; Stuttgart (Enke).
KÜSTER, W.F. (1985): Rechentafeln für die chemische Analytik.- 103. Aufl., 310 S.; Berlin (de Gruyter).
MENNE, B. (1996): Manganhaltige Ablagerungen in der Rettenbachhöhle (Kat.Nr. 1651/1, Oberösterreich) und ihre Zusammenhänge mit mikrobiologischen Prozessen.- Die Höhle, 47(3): 69- 74, 2 Tab.; Wien.
RÖMPPs Chemie- Lexikon.- 7. Aufl.; Stuttgart (Franckh).
SCHUSTER, R. (1992): Mineralogie.- Wiss. Berichte der Karstspeläologischen Arbeitsgemeinschaft Karlsruhe, 1: 68- 80, 1 Tab.; Karlsruhe.
SIMMLEIT, N. (1987): Klassifizierung und hydrochemische Charakterisierung von Tropfwässern am Beispiel zweier oberfränkischen Karsthöhlen.- Mitt. Verb. dt. Höhlen- u. Karstforsch., 33(2): 28- 31, 1 Abb., 3 Tab.; München.
SKINNER, H.C.W. & FITZPATRICK, R.W. [Hrsg.] (1992): Biomineralization, Processes of Iron and Manganese, Modern and Ancient Environments.- Catena Suppl., 21, 432 S.; Cremlingen.
TREIBER, D. (1984): Chemisches Praktikum, Technische Analyse, Versuche, Erläuterungen.- 104 S., Stuttgart (Selbstverlag).
ZIECHMANN, W. & MÜLLER- WEGENER, U. (1990): Bodenchemie.- 326 S.; Mannheim (B.I. Wissenschaftsverlag).